肥胖是一种世界性的流行病,它使人们容易患上许多与年龄有关的疾病,但它对器官功能障碍的确切影响在很大程度上尚不清楚。随着年龄的增长,毛囊干细胞(HFSCs)会减少,从而导致脱发。
在这里,作者报道了肥胖引起的压力,如高脂饮食(HFD)引起的压力,使HFSCs加速头发稀疏。
按时间顺序进行的基因表达分析显示,连续4天的HFD喂养将活化的HFSCs通过产生过量的活性氧诱导表皮角化,但没有减少HFSCs的数量。使用干细胞命运追踪、表观遗传学和反向遗传学的综合分析显示,进一步喂食HFD随后通过自分泌和/或旁分泌IL-1R信号通路诱导HFSCs内脂滴和NF-κB激活。
这些综合因素在HFSCs中显著抑制Sonic hedgehog (SHH)信号转导,从而通过异常分化进一步消耗富含脂质的HFSCs,并诱导毛囊小型化和最终脱发。这些综合因素在HFSCs中显著抑制Sonic hedgehog (SHH)信号转导,从而通过异常分化进一步消耗富含脂质的HFSCs,并诱导毛囊小型化和最终脱发。
这些数据共同表明,肥胖诱导的干细胞炎症信号强烈地抑制器官再生信号,以加速微型器官的微型化,并提示日常预防器官功能障碍的重要性。

肥胖使人易患许多与年龄有关的疾病,与人类的寿命密切相关。虽然许多器官因肥胖和/或老化而功能和结构衰退,但对于大多数器官来说,肥胖和/或高脂饮食是否直接影响器官功能和再生、针对哪些细胞群以及它们是如何发生的,目前尚不清楚。组织干细胞是器官稳态和衰老的基础。在毛发周期再生的增殖阶段(生长期)开始,膨大区域的HFSCs自我更新并产生分化的子代。
COL17A1是一种将HFSCs锚定在基膜上的半粒体成分,其与年龄相关的缺陷导致HFSCs通过表皮分化而耗尽,导致以干细胞为中心的毛囊老化,从而导致毛囊小型化和头发稀疏。虽然肥胖已被证明是人类雄激素性脱发(AGA)的一个危险因素,但它是专门针对AGA还是普遍诱导或加速脱发尚未进行测试。
首先,为了确定西方饮食(如HFD)是否会加速毛发脱落或稀疏,作者给20个月大的雄性C57BL/6N小鼠(未显示出明显毛发稀疏)喂食HFD或正常饮食(ND)一个月。这些结果表明,肥胖诱导的代谢应激加速了脱发。为了检测hfd喂养小鼠毛囊的整体结构,作者对COL17A1和K14进行了全贴式染色分析,分别鉴定了膨大细胞和基底细胞中的HFSCs。结果显示,hfd喂养的小鼠部分毛囊肿胀消失,有或没有保留较大的皮脂腺。结果证明肥胖似乎主要通过HFSCs的减少而显著加速头发的稀疏。
接下来,为了研究HFD诱导脱发的干细胞动力学,作者追踪了K15CrePR;Rosa-H2B-EGFP小鼠HFD喂养后GFP+ HFSCs的命运。在nd喂养的小鼠中,GFP+ HFSCs保留在鼓包中,其子代通过向下连续定位形成毛囊的循环部分,生长出毛干。相比之下,HFD喂养3个月后,GFP+ HFSCs在隆起部分减少,其后代在上部包括皮脂腺和交界区,也在表皮内连续定位。因此,hfd诱导的肥胖与HFSCs的循环激活协作,显著改变这些HFSCs的命运并消除它们。
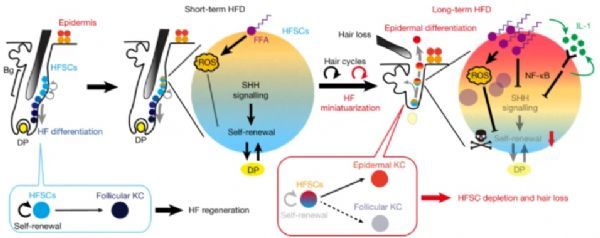
HFD诱导脱发的机制示意图
因为肥胖需要多轮头发周期来减少高果糖玉米糖的数量,肥胖不仅是脱发的一个危险因素,而且可能与重复的头发周期或衰老诱导的变化合作,显著地消除高果糖玉米糖的自我更新。这一机制加强了基于人类和小鼠研究的以干细胞为中心的器官衰老理论。在年轻动物体内的稳态中,HFSCs的表皮命运变化很少发生,但在伤口愈合过程中确实发生了短暂修复表皮的变化,这表明干细胞炎症信号可能是类似的生理过程的基础。
这项研究中的数据是用老鼠获得的,这在理解人类的机制方面有局限性,但结果表明,肥胖通常会增加人类患脱发的风险。饮食和肥胖对体细胞的显著影响表明通过生活方式管理日常器官功能障碍的重要性,并可能为治疗常见脱发和其他肥胖或年龄相关的再生缺陷和疾病开辟道路。
参考文献
Hironobu Morinaga et al. Obesity accelerates hair thinning by stem cell-centric converging mechanisms. Nature. 2021 Jun 23. doi: 10.1038/s41586-021-03624-x.